肌肉减少症(专业版)
肌肉减少症是指随着年龄增长而发生的肌肉质量减少、骨骼肌流失和肌肉功能强度下降等,这是人体衰老的重要标志。肌肉减少易引起骨折、关节损伤和跌倒等健康问题。
其他名称:衰老性少肌症,骨骼肌衰老,肌肉萎缩
英文名称:Sarcopenia,Sarcopenia with Aging
引起肌肉减少的风险因素主要包括如下:
调整饮食与生活方式
营养与草本综合干预
以下是基于循证医学和循证营养学有关文献综合的结果。
有助于防控少肌症的营养和草本补充剂,主要包括如下:
1.蛋白质和氨基酸:
增加蛋白质和氨基酸的摄入对于减缓并可能逆转肌肉损失至关重要1。当与运动相结合以及在恶病质早期实施时,增加蛋白质和氨基酸摄入对肌肉质量的益处可能更加明显1,2。
1).乳清蛋白和支链氨基酸:
单个氨基酸对健康和肌肉代谢有不同的影响,恶病质中氨基酸的最佳平衡尚不清楚。然而,支链氨基酸的亮氨酸、异亮氨酸和缬氨酸在促进肌肉组织生长方面尤其重要1,3。一些证据表明,每天摄入2-4g亮氨酸对刺激肌肉蛋白质合成尤其重要1-4。乳清蛋白补充剂富含亮氨酸和其他支链氨基酸,临床试验表明乳清蛋白可能有益于恶病质患者1,5。一项研究发现,与类似乳清蛋白的必需氨基酸和非必需氨基酸平衡补充剂相比,每天14g的必需氨基酸高亮氨酸混合物更有效地诱导健康志愿者和晚期癌症患者的蛋白质合成6。
一项安慰剂对照试验测试了富含亮氨酸的蛋白质补充剂对少肌症患者的影响。127名参加住院康复项目的老年人完成了这项研究。富含亮氨酸的乳清蛋白补充剂20g(提供2.8g亮氨酸),外加维生素、矿物质和膳食纤维。受试者服用这种混合物或等热量对照混合物,每天二次,持续四至八周。服用富含亮氨酸的乳清混合物的受试者在行走速度、肌肉质量和肌肉力量方面比服用对照混合物的受测者有更大的提高。此外,服用富含亮氨酸混合物的患者出院回家的比例更高,康复时间更短,康复强度更大7。
另一项对照试验包括46名患有中度至重度慢性阻塞性肺病(COPD)的男性,这种疾病通常与恶病质和肌肉萎缩有关。尽管体重没有显著变化,但与安慰剂相比,那些每天补充15.9g乳清蛋白加275mg镁和685mg维生素C治疗八周的患者,其无脂肪质量、身体蛋白质和握力增加,炎症细胞因子(IL-6)水平降低8。然而,在一项针对心力衰竭患者的试验中,在三个月内每天添加10g支链氨基酸并没有增加力量训练锻炼计划对肌肉力量和体能的积极影响,也没有增加对疲劳、躺下后头晕和呼吸急促等症状的积极影响9。
2). 大豆蛋白:
据报道,补充大豆蛋白与老年人的力量训练相结合,可以显著增加肌肉质量、力量和功能10,11。尽管长期以来,大豆和其他植物蛋白一直被认为比乳清和其他动物蛋白具有较弱的肌肉增强作用,因为它们的必需氨基酸含量相对较低,包括亮氨酸12-14,但一项对266名参与者的九项试验的荟萃分析发现,大豆蛋白和乳清蛋白与力量增强运动相结合,在肌肉质量和力量方面产生了类似的增长15。在一项针对健康男性和女性的研究中,在为期12周的力量训练计划中,补充19g乳清蛋白分离物或26g大豆蛋白分离物,其中提供约2g亮氨酸,可导致相同程度的肌肉生长16。
另一种可能改善大豆蛋白效果的策略是用亮氨酸代谢产物HMB强化。在一项有8名参与者参加的小型交叉试验中,禁食36小时后的肌肉生长通过每天3g HMB强化的大豆蛋白补充剂和富含亮氨酸的乳清蛋白补充剂得到了类似的增强17。尽管很少有研究表明大豆蛋白对恶病质的影响,但一项安慰剂对照试验包括73名体表面积为20-50%的烧伤患者,发现用大豆蛋白分离物治疗三周可以减少体重,增加肌肉保留18。除了增加肌肉蛋白合成外,大豆蛋白还可以改善心血管和代谢健康,一些证据表明,在与恶病质相关的条件下,大豆中发现的蛋白酶抑制剂可能有助于缓解肌肉崩溃19-21。
3). 鸡蛋和其他蛋白质:
鸡蛋、肉和鱼是高质量蛋白质的来源,这些蛋白质与成年人更大的肌肉质量有关22。然而,在一项对36名老年受试者进行的为期12周的力量训练项目的临床试验中,每公斤体重提供1.2g蛋白质的饮食(主要来自鸡蛋、肉类和乳制品)对肌肉质量的影响与每公斤体重0.9g蛋白质的膳食相同23。
鸡蛋蛋白富含亮氨酸和支链氨基酸,因此可能对老年人和那些可能导致肌肉萎缩的人的肌肉生长和维持产生积极影响24,25。然而,动物研究结果表明,乳清蛋白在刺激肌肉生长方面可能比鸡蛋蛋白更有效26。
2. 羟甲基丁酸钙(HMB):
在健康成年人和老年人的试验中,亮氨酸的代谢产物HMB已被证明可以增加肌肉蛋白合成并抑制肌肉分解,尤其是与运动结合时27,28。在一项针对老年女性的安慰剂对照试验中,含有2g HMB、5g精氨酸和1.5g赖氨酸的补充剂比安慰剂增加了20%的全身蛋白质合成,增加了肌肉大小和力量,并改善了“站起来就走”的功能29。在另一项针对77名老年参与者的试验中,与提供等量氮的对照补充剂相比,服用HMB加精氨酸和赖氨酸可使瘦体重增加1.2%30。
其他临床研究表明,需要足够的维生素D来支持HMB/精氨酸/赖氨酸对肌肉力量的积极影响,但不支持肌肉质量31。HMB每天3g,加上精氨酸和谷氨酰胺每天14g,也被发现会增加因癌症和艾滋病毒/艾滋病而肌肉萎缩的人的体重和无脂肪体重32,33。一项对患有经常与肌肉萎缩相关疾病的老年参与者进行的15项随机对照试验的荟萃分析得出结论,每天3g HMB单独或与其他氨基酸一起治疗四周或更长时间,可以在不影响体重的情况下诱导肌肉力量和质量的小幅增加34。
3. L-肉碱:
L-肉碱是一种存在于肉类中的氨基酸衍生物,可以在体内少量合成。肉碱通过两种方式在能量生产中发挥关键作用:1)肉碱化合物通过线粒体膜运输脂肪,在线粒体膜上燃烧脂肪以获取能量;2)肉碱上调几种能量生产反应。
在心力衰竭患者中,肉碱不足与少肌症的关系比与骨骼肌力减退症的关系更密切,这表明肉碱不足是这些患者少肌症潜在的治疗靶点35。
在一项回顾性文献中,作者指出:L-肉碱似乎可以剂量依赖性地抑制少肌症的进展,这与肝硬化患者高氨血症的改善有关36。
4. 肌酸:
肌酸是健美运动员常用的一种类似氨基酸的化合物,也可能用于治疗肌肉萎缩。肌酸存在于肉类和鱼类中,人体每天从甘氨酸、精氨酸和蛋氨酸中产生约1-2g肌酸。
许多研究报告说,老年人的肌肉肌酸水平低于年轻人;然而,每天补充5-20g肌酸可以显著提高老年人的肌肉肌酸水平。在2011年的一项综述中,7项已发表的研究中有4项(57%)报告称,每天补充约5至20g肌酸(通常在一天中以3个相等剂量给予)可显著提高接受重量训练计划的老年人的力量37。一项针对35名老年男性的10周重量训练项目研究报告称,与安慰剂组5.5%的肌肉厚度增加相比,低剂量(每天0.1g/kg)肌酸组的平均肌肉厚度增加了10.4%38。
5.欧米伽3脂肪酸:
欧米伽3脂肪酸存在于在某些高脂肪鱼类和鱼油中,一些种子和坚果包括核桃、亚麻籽和奇亚籽等含量丰富。摄入足量的ω-3脂肪酸有助于预防和治疗分解代谢消耗。
在一项试验中,20名健康的年轻女性每天服用5g的Omega-3脂肪酸,或一种对照油,在她们的一条腿被固定两周之前的四周开始。与对照组相比,服用Omega-3补充剂的女性肌肉体积损失更少,而且欧米伽-3组的肌肉蛋白质合成更多39。在一项针对16名健康老年人的研究中,与每天摄入4g玉米油的对照组参与者相比,在8周内每天摄入4g Omega-3补充剂(含有1.86g EPA和1.5g DHA)与显著更高的蛋白质合成率有关40。
英国一项针对2983名老年人的研究报告称,食用高脂肪鱼类与握力更强有关41。在一项针对18名癌症恶病质患者的研究中,研究人员报告称,患者每天服用约12g鱼油(含18%的EPA和12%的DHA),平均每月体重增加约0.32kg。在补充之前,这些患者严重恶病质,平均每月减轻2.9kg42。
6.维生素D:
维生素D是维持免疫力以及肌肉和骨骼生长和维持的关键营养素。维生素D缺乏症很常见,一项针对3170名≥60岁的美国成年人的研究报告称,约76%的白人、96%的黑人和92%的墨西哥裔美国人的维生素D水平<30ng/mL43。众所周知,维生素D可以增强肌肉力量,在老年人中,维生素D的剂量为700-1200IU/天时,它可以显著降低跌倒几率44,45。
荷兰一项针对127名老年人的研究发现,维生素D水平低(<20ng/mL)与瘦体重减少和体能受损有关46。在另一项研究中,4000多名70-88岁的男性在基线测量维生素D水平后,平均随访5.3年。在维生素D水平约为21ng/mL或更低的男性中,基线时虚弱的患病率比维生素D水平大于32ng/mL的男性高96%。对于那些在基线时并不虚弱的男性,与维生素D水平最高的男性相比,维生素D水平低的男性在5.3年的随访期内变得虚弱的风险高出56%47。一般建议大多数人将血液中25-羟基维生素D的水平保持在50至80ng/mL之间,以获得最佳健康。
7.共轭亚油酸:
许多动物和人类研究报告称,摄入共轭亚油酸(CLA)与较高的瘦体重和/或较低的脂肪量有关。一项研究报告称在小鼠饮食中添加0.5%的CLA与显著较高的瘦肌肉量有关48。
一项为期6个月的安慰剂对照研究每天用6g CLA和5g肌酸治疗老年人。所有受试者都参加了每周两次的举重项目。6个月后,补充CLA肌酸的组比安慰剂组明显增加了更多的瘦体重(2.1kg对0.91kg),减少了更多的脂肪重量(1.9kg对0.41kg)49。
8.矿物质:
充足的矿物质摄入对保持老年人的肌肉质量也很重要。许多老年人的饮食摄入量和/或血液中几种矿物质(包括钙、镁、硒、铬和锌)水平不足50,51。
一项针对1339名60岁以上韩国成年人的研究报告称,与钙摄入量较低的成年人相比,每日钙摄入量较高与脂肪量显著减少、肌肉量增加和少肌症风险降低有关52。一项针对740名50岁以上塔斯马尼亚成年人的研究报告称,铁、镁、磷、钾和锌的摄入量越高,其手臂和腿部的瘦肌肉量就越大53。动物研究报告称,锌缺乏会降低食欲,较高水平的膳食和补充锌会增加食欲54。
许多恶病质或少肌症患者也会出现骨量减少(骨质疏松症或骨质减少)。一些研究人员指出,少肌症和绝经后骨质疏松症共存,具有非常相似的风险因素,在疾病发展方面表现出相似性,并相互作用55。骨质疏松症大大增加了骨折的风险,髋部和背部骨折通常很少或没有创伤。对63项研究中29项的分析 897名50岁以上的成年人报告称,每天补充800-1500mg钙和400-800IU维生素D可显著降低12%的骨质疏松症相关骨折56。
9.益生菌与慢性腹泻:
艾滋病HIV阳性个体或接受癌症放疗或化疗的人经常经历慢性腹泻,这会显著减少对许多营养物质的吸收。几项研究报告称,使用嗜酸乳杆菌和长双歧杆菌等益生菌可以显著降低艾滋病毒/艾滋病或癌症辐射相关腹泻的发病率57,58。一项针对患有HIV/AIDS相关中度腹泻的女性的研究报告称,在所有12名女性中,每天食用100ml(约3.5盎司)补充有鼠李糖乳杆菌GR1和罗伊氏乳杆菌RC-14的酸奶15天,可以缓解腹泻。每天接受100ml普通酸奶的12名女性中,只有2名(17%)腹泻症状得到缓解。给予两组女性的酸奶最初是用低水平的2种细菌制备的,包括保加利亚德氏乳杆菌和嗜热链球菌57。
对490名接受过结直肠癌或宫颈癌症放射治疗的患者进行了一项大型双盲研究。这些患者接受了含有4500亿活细菌的益生菌补充剂(含有8株益生菌的混合物:ACTIAL益生菌专有品牌VSL#3)或安慰剂在放射治疗期间每天3次。243名接受益生菌治疗的患者中有77名(31.6%)发生了辐射诱导的腹泻,这明显低于239名接受安慰剂治疗的患者(51.8%)中的124名59。
益生菌的混合物在预防腹泻方面可能比单独的益生菌更有用。在对16项已发表的关于益生菌对几种医疗条件(包括肠道健康、预防呼吸道感染、特应性皮炎和腹泻)影响的研究进行综述时,12项研究发现,益生菌混合物比使用单一益生菌菌株更有效60。
10.消化酶:
肌肉萎缩的人也可能受益于口服消化酶补充剂。许多研究报告称,与年轻人相比,老年人的胰腺酶(即消化蛋白质、脂肪和碳水化合物的酶)水平更低61。报告了3名成年人(年龄78至80岁,无胰腺病史)的一系列病例,他们经历了慢性腹泻或呕吐以及严重的体重减轻。服用消化酶后,腹泻和呕吐症状缓解,患者在1至10个月内体重增加了5.9kg至13.6kg62。
另一项研究报告称,在22名服用抗病毒药物并患有慢性腹泻的HIV阳性患者中,有8人的胰腺消化酶水平较低。一名患者在研究期间死于艾滋病毒/艾滋病相关疾病。另外7名患者在接受10, 000至60, 000单位的胰腺酶治疗后,腹泻显著减少63。在另一项针对24名患有严重脂肪吸收不良(即粪便中的脂肪或脂肪泻)的HIV/AIDS患者的研究中,受试者每摄入1g脂肪,就要接受1000单位脂肪酶、800单位淀粉酶和60单位蛋白酶的治疗。经过2周的酶治疗,8名患者(33%)的脂肪吸收不良得到缓解,另外11名患者(46%)的脂肪吸收不良得到显著改善64。
更多内容可点击其个性化的综合干预方案:
以及参阅本网如下专文的有关内容:
医疗干预
在医生监督下,治疗措施包括如下:
参考文献:
1. Prado CMM et al. Nutrition interventions to treat low muscle mass in cancer. J Cachexia Sarcopenia Muscle. 2020;11(2): 366-380.
2. Antoun S et al. Muscle protein anabolism in advanced cancer patients: response to protein and amino acids support, and to physical activity. Ann Oncol. 2018;29(suppl_2): ii10-ii17.
3. de Campos-Ferraz PL et al. An overview of amines as nutritional supplements to counteract cancer cachexia. J Cachexia Sarcopenia Muscle. 2014;5(2): 105-110.
4. Soares JDP et al. Dietary Amino Acids and Immunonutrition Supplementation in Cancer-Induced Skeletal Muscle Mass Depletion: A Mini-Review. Curr Pharm Des. 2020;26(9): 970-978.
5. Teixeira FJ et al. Whey protein in cancer therapy: A narrative review. Pharmacol Res. 2019;144: 245-256.
6. Engelen MAM et al. High anabolic potential of essential amino acid mixtures in advanced nonsmall cell lung cancer. Ann Oncol. 2015;26(9): 1960-1966.
7. Rondanelli ME et al. Caccialanza and S. Perna. Improving rehabilitation in sarcopenia: a randomized-controlled trial utilizing a muscle-targeted food for special medical purposes. J Cachexia Sarcopenia Muscle. 2020;11(6): 1535-1547.
8. Ahmadi AMH et al. Fortified whey beverage for improving muscle mass in chronic obstructive pulmonary disease: a single-blind, randomized clinical trial. Respir Res.2020;21(1): 216.
9. Pineda-Juárez JA et al. Changes in body composition in heart failure patients after a resistance exercise program and branched chain amino acid supplementation. Clin Nutr. 2016;35(1): 41-47.
10. Orsatti FL et al. Adding Soy Protein to Milk Enhances the Effect of Resistance Training on Muscle Strength in Postmenopausal Women. J Diet Suppl. 2018;15(2): 140-152.
11. Liao YH et al. Soymilk ingestion immediately after therapeutic exercise enhances rehabilitation outcomes in chronic stroke patients: A randomized controlled trial. NeuroRehabilitation. 2019;44(2): 217-229.
12. Devries MC et al. Supplemental protein in support of muscle mass and health: advantage whey. J Food Sci. 2015;80 Suppl 1: A8-a15.
13. van Vliet S et al. The Skeletal Muscle Anabolic Response to Plant- versus Animal-Based Protein Consumption. J Nutr. 2015;145(9): 1981-1991.
14. Devries MC et al. Protein leucine content is a determinant of shorter- and longer-term muscle protein synthetic responses at rest and following resistance exercise in healthy older women: a randomized, controlled trial. Am J Clin Nutr. 2018;107(2): 217-226.
15. Messina M et al. No Difference Between the Effects of Supplementing With Soy Protein Versus Animal Protein on Gains in Muscle Mass and Strength in Response to Resistance Exercise. Int J Sport Nutr Exerc Metab. 2018;28(6): 674-685.
16. Lynch HM et al. No Significant Differences in Muscle Growth and Strength Development When Consuming Soy and Whey Protein Supplements Matched for Leucine Following a 12 Week Resistance Training Program in Men and Women: A Randomized Trial. Int J Environ Res Public Health. 2020;17(11).
17. Rittig N et al. Anabolic effects of leucine-rich whey protein, carbohydrate, and soy protein with and without β-hydroxy-β-methylbutyrate (HMB) during fasting-induced catabolism: A human randomized crossover trial. Clin Nutr. 2017;36(3): 697-705.
18. Babajafari S et al. Comparing isolated soy protein with flaxseed oil vs isolated soy protein with corn oil and wheat flour with corn oil consumption on muscle catabolism, liver function, blood lipid, and sugar in burn patients: a randomized clinical trial. Trials. 2018;19(1): 308.
19. Nikawa T et al. Effects of a soy protein diet on exercise-induced muscle protein catabolism in rats. Nutrition. 2002;18(6): 490-495.
20. Morris CA et al. Attenuation of skeletal muscle atrophy via protease inhibition. J Appl Physiol. 2005;(1985) 99(5): 1719-1727.
21. Paul et al. Evidence Supports the Use of Soy Protein to Promote Cardiometabolic Health and Muscle Development. J Am Coll Nutr. 2015;34 Suppl 1: 56-59.
22. Alexandrov NV et al. Dietary Protein Sources and Muscle Mass over the Life Course: The Lifelines Cohort Study. Nutrients. 2018;10(10).
23. Bhasin S et al. Effect of Protein Intake on Lean Body Mass in Functionally Limited Older Men: A Randomized Clinical Trial. JAMA Intern Med. 2018;178(4): 530-541
24. Miranda JM et al. Egg and egg-derived foods: effects on human health and use as functional foods. Nutrients. 2015;7(1): 706-729.
25. Smith A et al. Considering the benefits of egg consumption for older people at risk of sarcopenia. Br J Community Nurs. 2016;21(6): 305-309.
26. Mobley EB et al. Effects of protein type and composition on postprandial markers of skeletal muscle anabolism, adipose tissue lipolysis, and hypothalamic gene expression. J Int Soc Sports Nutr. 2015;12: 14.
27. Molfino A et al. Beta-hydroxy-beta-methylbutyrate supplementation in health and disease: a systematic review of randomized trials. Amino Acids. 2013;45(6): 1273-1292.
28. Holeček M. Beta-hydroxy-beta-methylbutyrate supplementation and skeletal muscle in healthy and muscle-wasting conditions. J Cachexia Sarcopenia Muscle. 2017;8(4): 529-541.
29. Flakoll P et al. Effect of beta-hydroxy-beta-methylbutyrate, arginine, and lysine supplementation on strength, functionality, body composition, and protein metabolism in elderly women. Nutrition. 2004;20(5): 445-451.
30. Baier S et al. Year-long changes in protein metabolism in elderly men and women supplemented with a nutrition cocktail of beta-hydroxy-beta-methylbutyrate (HMB), L-arginine, and L-lysine. JPEN J Parenter Enteral Nutr. 2009 Jan-Feb;33(1):71-82.
31. Fuller JC et al. Vitamin D status affects strength gains in older adults supplemented with a combination of β-hydroxy-β-methylbutyrate, arginine, and lysine: a cohort study. JPEN J Parenter Enteral Nutr. 2011;35(6): 757-762.
32. Clark R et al. Nutritional treatment for acquired immunodeficiency virus-associated wasting using HMB, glutamine and arginine: A double-blind, placebo controlled study. JPEN - J Parenter Enter Nutr 2000;24(3):133-139.
33. May PE et al. Reversal of cancer-related wasting using oral supplementation with a combination of beta-hydroxy-beta-methylbutyrate, arginine, and glutamine. Am J Surg. 2002 Apr;183(4):471-9.
34. Bear DE et al. β-Hydroxy-β-methylbutyrate and its impact on skeletal muscle mass and physical function in clinical practice: a systematic review and meta-analysis. Am J Clin Nutr. 2019;109(4): 1119-1132.
35. Kinugasa Y et al. Association of carnitine insufficiency with sarcopenia and dynapenia in patients with heart failure. Geriatr Gerontol Int. 2023 Jul;23(7):524-530.
36. Hiramatsu A et al. Levocarnitine Use Is Associated With Improvement in Sarcopenia in Patients With Liver Cirrhosis. Hepatol Commun. 2019 Jan 22;3(3):348-355.
37. Rawson ES et al. Use of creatine and evidence for effects of cognitive function in the young and old. Amino Acids 2011;40(5):1349-1362.
38. Candow DG et al. Low-dose creatine combined with protein during resistance training in older men. Med Sci Sports Exerc 2008;40(9):1645-1652.
39. McGlory C et al. Omega-3 fatty acid supplementation attenuates skeletal muscle disuse atrophy during two weeks of unilateral leg immobilization in healthy young women. The FASEB Journal. 2019;33(3):4586-4597.
40. Smith GI et al. Dietary omega-3 fatty acid supplementation increases the rate of muscle protein synthesis in older adults: a randomized controlled trial. Am J Clin Nutr 2011;93(2):402-412.
41. Robinson SM et al. Diet and its relationship with grip strength in community-dwelling older men and women: the Hertfordshire Cohort Study. J Am Geriatr Soc 2008;56(1):84-90.
42. Wigmore SJ et al. The effect of polyunsaturated fatty acids with the progress of cachexia in patients with pancreatic cancer. Nutrition 1996;12 (supplement 1):S27-S30.
43. Ginde AA et al. Demographic differences and trends of vitamin D insufficiency in the US population. Arch Int Med 2009;169:629-632.
44. Bischoff-Ferrari A et al. Fall prevention with supplemental and active forms of vitamin D: a meta-analysis of randomized controlled trials. BMJ 2009;339:b3692.
45. Dawson-Hughes B. Serum 25-hydroxyvitamin D and functional outcomes in the elderly. Am J Clin Nutr 2008;88(supplement):537S-540S.
46. Tieland M et al. Low vitamin D status is associated with reduced muscle mass and impaired physical performance in frail elderly people. European journal of clinical nutrition. Oct 2013;67(10):1050-1055.
47. Wong YY et al. Low vitamin D status is an independent predictor of increased frailty and all-cause mortality in older men: the Health in Men Study. The Journal of clinical endocrinology and metabolism. Sep 2013;98(9):3821-3828.
48. Rahman MM et al. Conjugated linoleic acid (CLA) prevents age associated skeletal muscle loss. Biochem Biophys Res Commun 2009;383(4):513-518.
49. Tarnopolsky M et al. Creatine monohydrate and conjugated linoleic acid improve strength and body composition following resistance exercise in older adults. PLoS One 2007;2(10):e991.
50. Park S et al. Vitamin and mineral supplements: Barrier and challenges for older adults. J Nutr Elderly 2008;27(3-4):297-317.
51. Vaquero MP. Magnesium and trace elements in the elderly: Intake, status, and recommendations. J Nutr Health Aging 2002;6(2):147-153.
52. Seo MH et al. The association between daily calcium intake and sarcopenia in older, non-obese Korean adults: the Fourth Korea National Health and Nutrition Examination Survey (KNHANES IV) 2009. Endocr J 2013;60(5):679-686.
53. Scott D et al. Associations between dietary nutrient intake and muscle mass and strength in community-dwelling older adults: The Tasmanian older adult cohort study. J Am Geriatr Soc 2010;58:2129-2134.
54. Suzuki H et al. Zinc as an appetite stimulator- the possible role of zinc in the progression of diseases such as cachexia and sarcopenia. Recent Pat Food Nutr Agric 2011;3(3):226-231.
55. Sirola J et al. Similarities in acquired factors related to postmenopausal osteoporosis and sarcopenia. J Osteroporos 2011. Doi: 4061/2011/536735
56. Tang B et al. Use of calcium in combination with vitamin D supplementation to prevent fractures and bone loss in people aged 50 years or older: a meta-analysis. Lancet 2007;370(9844):657-666.
57. Anukam KC et al. Yogurt containing probiotic Lactobacillus rhamnosus GR-1 and L. reuteri RC-14 helps resolve moderate diarrhea and increases CD4 count in HIV/ AIDS patients. J Clin Gastroenterol 2008; 42(3):239-243.
58. Fuccio L et al. Effects of probiotics for the prevention and treatment of radiation-induced diarrhea. J Clin Gastroenterol 2009;43(5):506-513.
59. Delia P et al. Use of probiotics for prevention of radiation-induced diarrhea. World J Gastroenterol 2007;13:912-915.
60. Chapman CMC et al. Health benefits of probiotics: are mixtures more effective than single strains? Eur J Nutr 2011;50:1-17.
61. Holt PR. Intestinal malabsorption in the elderly. Dig Dis 2007;144-150.
62. Coulson JM et al. Pancreatic insufficiency and weight loss in older patients. QJM (Quartely Journal of Medicine) 2004;97:377-380.
63. Price DA et al. Pancreatic exocrine unsufficiency in HIV-positive patients. HIV Medicine 2005;6:33-36.
64. Carrocio A et al. Efficacy of oral pancreatic enzyme therapy for the treatment of fat malabsorption in HIV-infected patients. Aliment Pharmacol Ther 2001;15:1619-1625.
美国国立公众健康网
https://medlineplus.gov
美国医疗在线网
www.webmd.com
维基百科-少肌症
https://en.wikipedia.org/wiki/Sarcopenia
美国国际少肌症论坛
https://frailty-sarcopenia.com/
美国国立卫生研究院
www.nih.gov
免责声明和安全信息
英文名称:Sarcopenia,Sarcopenia with Aging
定义
肌肉减少症是指随着年龄增长而发生的肌肉质量减少、骨骼肌流失和肌肉功能强度下降等,这是人体衰老的重要标志。肌肉减少易引起骨折、关节损伤和跌倒等健康问题。肌肉质量下降也可导致心脏和肺部功能下降、衰竭,甚至死亡。病因
机体老化是少肌症的主因,一般认为存在下列因素:- 炎症(细胞因子)影响作用,炎症介质改变了许多代谢过程,导致肌肉蛋白合成减少和肌肉蛋白质分解增加,使肌肉逐渐散失
- 氧化损伤、线粒体功能障碍
- 血管和神经功能障碍
- 激素水平降低,如生长激素、胰岛素样生长因子(IGF-1)和睾酮水平
- 胰岛素抵抗
风险因素
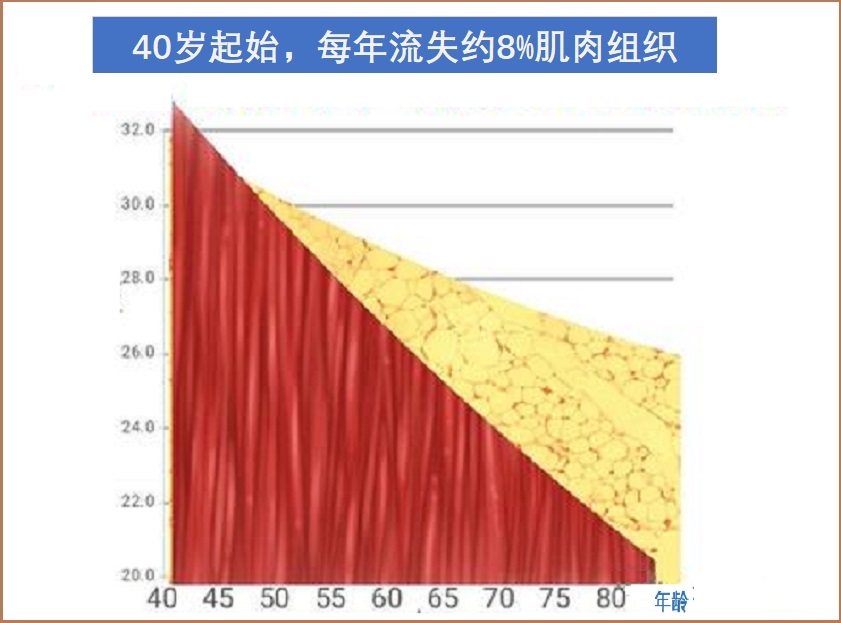
从出生以后,人体肌肉不断增长且强壮有力。大约在40岁左右,肌肉质量和功能开始下降和流失。引起肌肉减少的风险因素主要包括如下:
- 机体老化,使肌肉质量下降和功能丧失,60岁开始明显加快
- 营养不良,尤其蛋白质摄入不足
- 身体活动少,如果缺乏身体活动,每10年可失去3-5%肌肉
- 心脏疾病
- 慢性肾病(肾功能衰竭)
- 慢性肝病
- 2型糖尿病,加速肌肉流失
症状
少肌症的主要症状包括:- 肌肉质量减少
- 肌肉无力、疲劳
- 手握力量降低
- 步行速度减慢
并发症
随着年龄老化,少肌症可能导致如下并发症:- 骨折或关节受损
- 站立困难、跌倒
- 步履缓慢
- 器官功能退化,如心脏、肺部衰竭
疗法
综合选项包括如下:调整饮食与生活方式
- 富含高蛋白的饮食,如瘦肉、鱼肉等
- 新鲜蔬菜、水果等,富含抗氧化剂,降低炎性因子
- 坚持运动锻炼,如经常快步行走等。
- 负重运动(阻力训练),结合蛋白营养补充
- 不抽烟,或戒烟
营养与草本综合干预
以下是基于循证医学和循证营养学有关文献综合的结果。
有助于防控少肌症的营养和草本补充剂,主要包括如下:
1.蛋白质和氨基酸:
增加蛋白质和氨基酸的摄入对于减缓并可能逆转肌肉损失至关重要1。当与运动相结合以及在恶病质早期实施时,增加蛋白质和氨基酸摄入对肌肉质量的益处可能更加明显1,2。
1).乳清蛋白和支链氨基酸:
单个氨基酸对健康和肌肉代谢有不同的影响,恶病质中氨基酸的最佳平衡尚不清楚。然而,支链氨基酸的亮氨酸、异亮氨酸和缬氨酸在促进肌肉组织生长方面尤其重要1,3。一些证据表明,每天摄入2-4g亮氨酸对刺激肌肉蛋白质合成尤其重要1-4。乳清蛋白补充剂富含亮氨酸和其他支链氨基酸,临床试验表明乳清蛋白可能有益于恶病质患者1,5。一项研究发现,与类似乳清蛋白的必需氨基酸和非必需氨基酸平衡补充剂相比,每天14g的必需氨基酸高亮氨酸混合物更有效地诱导健康志愿者和晚期癌症患者的蛋白质合成6。
一项安慰剂对照试验测试了富含亮氨酸的蛋白质补充剂对少肌症患者的影响。127名参加住院康复项目的老年人完成了这项研究。富含亮氨酸的乳清蛋白补充剂20g(提供2.8g亮氨酸),外加维生素、矿物质和膳食纤维。受试者服用这种混合物或等热量对照混合物,每天二次,持续四至八周。服用富含亮氨酸的乳清混合物的受试者在行走速度、肌肉质量和肌肉力量方面比服用对照混合物的受测者有更大的提高。此外,服用富含亮氨酸混合物的患者出院回家的比例更高,康复时间更短,康复强度更大7。
另一项对照试验包括46名患有中度至重度慢性阻塞性肺病(COPD)的男性,这种疾病通常与恶病质和肌肉萎缩有关。尽管体重没有显著变化,但与安慰剂相比,那些每天补充15.9g乳清蛋白加275mg镁和685mg维生素C治疗八周的患者,其无脂肪质量、身体蛋白质和握力增加,炎症细胞因子(IL-6)水平降低8。然而,在一项针对心力衰竭患者的试验中,在三个月内每天添加10g支链氨基酸并没有增加力量训练锻炼计划对肌肉力量和体能的积极影响,也没有增加对疲劳、躺下后头晕和呼吸急促等症状的积极影响9。
2). 大豆蛋白:
据报道,补充大豆蛋白与老年人的力量训练相结合,可以显著增加肌肉质量、力量和功能10,11。尽管长期以来,大豆和其他植物蛋白一直被认为比乳清和其他动物蛋白具有较弱的肌肉增强作用,因为它们的必需氨基酸含量相对较低,包括亮氨酸12-14,但一项对266名参与者的九项试验的荟萃分析发现,大豆蛋白和乳清蛋白与力量增强运动相结合,在肌肉质量和力量方面产生了类似的增长15。在一项针对健康男性和女性的研究中,在为期12周的力量训练计划中,补充19g乳清蛋白分离物或26g大豆蛋白分离物,其中提供约2g亮氨酸,可导致相同程度的肌肉生长16。
另一种可能改善大豆蛋白效果的策略是用亮氨酸代谢产物HMB强化。在一项有8名参与者参加的小型交叉试验中,禁食36小时后的肌肉生长通过每天3g HMB强化的大豆蛋白补充剂和富含亮氨酸的乳清蛋白补充剂得到了类似的增强17。尽管很少有研究表明大豆蛋白对恶病质的影响,但一项安慰剂对照试验包括73名体表面积为20-50%的烧伤患者,发现用大豆蛋白分离物治疗三周可以减少体重,增加肌肉保留18。除了增加肌肉蛋白合成外,大豆蛋白还可以改善心血管和代谢健康,一些证据表明,在与恶病质相关的条件下,大豆中发现的蛋白酶抑制剂可能有助于缓解肌肉崩溃19-21。
3). 鸡蛋和其他蛋白质:
鸡蛋、肉和鱼是高质量蛋白质的来源,这些蛋白质与成年人更大的肌肉质量有关22。然而,在一项对36名老年受试者进行的为期12周的力量训练项目的临床试验中,每公斤体重提供1.2g蛋白质的饮食(主要来自鸡蛋、肉类和乳制品)对肌肉质量的影响与每公斤体重0.9g蛋白质的膳食相同23。
鸡蛋蛋白富含亮氨酸和支链氨基酸,因此可能对老年人和那些可能导致肌肉萎缩的人的肌肉生长和维持产生积极影响24,25。然而,动物研究结果表明,乳清蛋白在刺激肌肉生长方面可能比鸡蛋蛋白更有效26。
2. 羟甲基丁酸钙(HMB):
在健康成年人和老年人的试验中,亮氨酸的代谢产物HMB已被证明可以增加肌肉蛋白合成并抑制肌肉分解,尤其是与运动结合时27,28。在一项针对老年女性的安慰剂对照试验中,含有2g HMB、5g精氨酸和1.5g赖氨酸的补充剂比安慰剂增加了20%的全身蛋白质合成,增加了肌肉大小和力量,并改善了“站起来就走”的功能29。在另一项针对77名老年参与者的试验中,与提供等量氮的对照补充剂相比,服用HMB加精氨酸和赖氨酸可使瘦体重增加1.2%30。
其他临床研究表明,需要足够的维生素D来支持HMB/精氨酸/赖氨酸对肌肉力量的积极影响,但不支持肌肉质量31。HMB每天3g,加上精氨酸和谷氨酰胺每天14g,也被发现会增加因癌症和艾滋病毒/艾滋病而肌肉萎缩的人的体重和无脂肪体重32,33。一项对患有经常与肌肉萎缩相关疾病的老年参与者进行的15项随机对照试验的荟萃分析得出结论,每天3g HMB单独或与其他氨基酸一起治疗四周或更长时间,可以在不影响体重的情况下诱导肌肉力量和质量的小幅增加34。
3. L-肉碱:
L-肉碱是一种存在于肉类中的氨基酸衍生物,可以在体内少量合成。肉碱通过两种方式在能量生产中发挥关键作用:1)肉碱化合物通过线粒体膜运输脂肪,在线粒体膜上燃烧脂肪以获取能量;2)肉碱上调几种能量生产反应。
在心力衰竭患者中,肉碱不足与少肌症的关系比与骨骼肌力减退症的关系更密切,这表明肉碱不足是这些患者少肌症潜在的治疗靶点35。
在一项回顾性文献中,作者指出:L-肉碱似乎可以剂量依赖性地抑制少肌症的进展,这与肝硬化患者高氨血症的改善有关36。
4. 肌酸:
肌酸是健美运动员常用的一种类似氨基酸的化合物,也可能用于治疗肌肉萎缩。肌酸存在于肉类和鱼类中,人体每天从甘氨酸、精氨酸和蛋氨酸中产生约1-2g肌酸。
许多研究报告说,老年人的肌肉肌酸水平低于年轻人;然而,每天补充5-20g肌酸可以显著提高老年人的肌肉肌酸水平。在2011年的一项综述中,7项已发表的研究中有4项(57%)报告称,每天补充约5至20g肌酸(通常在一天中以3个相等剂量给予)可显著提高接受重量训练计划的老年人的力量37。一项针对35名老年男性的10周重量训练项目研究报告称,与安慰剂组5.5%的肌肉厚度增加相比,低剂量(每天0.1g/kg)肌酸组的平均肌肉厚度增加了10.4%38。
5.欧米伽3脂肪酸:
欧米伽3脂肪酸存在于在某些高脂肪鱼类和鱼油中,一些种子和坚果包括核桃、亚麻籽和奇亚籽等含量丰富。摄入足量的ω-3脂肪酸有助于预防和治疗分解代谢消耗。
在一项试验中,20名健康的年轻女性每天服用5g的Omega-3脂肪酸,或一种对照油,在她们的一条腿被固定两周之前的四周开始。与对照组相比,服用Omega-3补充剂的女性肌肉体积损失更少,而且欧米伽-3组的肌肉蛋白质合成更多39。在一项针对16名健康老年人的研究中,与每天摄入4g玉米油的对照组参与者相比,在8周内每天摄入4g Omega-3补充剂(含有1.86g EPA和1.5g DHA)与显著更高的蛋白质合成率有关40。
英国一项针对2983名老年人的研究报告称,食用高脂肪鱼类与握力更强有关41。在一项针对18名癌症恶病质患者的研究中,研究人员报告称,患者每天服用约12g鱼油(含18%的EPA和12%的DHA),平均每月体重增加约0.32kg。在补充之前,这些患者严重恶病质,平均每月减轻2.9kg42。
6.维生素D:
维生素D是维持免疫力以及肌肉和骨骼生长和维持的关键营养素。维生素D缺乏症很常见,一项针对3170名≥60岁的美国成年人的研究报告称,约76%的白人、96%的黑人和92%的墨西哥裔美国人的维生素D水平<30ng/mL43。众所周知,维生素D可以增强肌肉力量,在老年人中,维生素D的剂量为700-1200IU/天时,它可以显著降低跌倒几率44,45。
荷兰一项针对127名老年人的研究发现,维生素D水平低(<20ng/mL)与瘦体重减少和体能受损有关46。在另一项研究中,4000多名70-88岁的男性在基线测量维生素D水平后,平均随访5.3年。在维生素D水平约为21ng/mL或更低的男性中,基线时虚弱的患病率比维生素D水平大于32ng/mL的男性高96%。对于那些在基线时并不虚弱的男性,与维生素D水平最高的男性相比,维生素D水平低的男性在5.3年的随访期内变得虚弱的风险高出56%47。一般建议大多数人将血液中25-羟基维生素D的水平保持在50至80ng/mL之间,以获得最佳健康。
7.共轭亚油酸:
许多动物和人类研究报告称,摄入共轭亚油酸(CLA)与较高的瘦体重和/或较低的脂肪量有关。一项研究报告称在小鼠饮食中添加0.5%的CLA与显著较高的瘦肌肉量有关48。
一项为期6个月的安慰剂对照研究每天用6g CLA和5g肌酸治疗老年人。所有受试者都参加了每周两次的举重项目。6个月后,补充CLA肌酸的组比安慰剂组明显增加了更多的瘦体重(2.1kg对0.91kg),减少了更多的脂肪重量(1.9kg对0.41kg)49。
8.矿物质:
充足的矿物质摄入对保持老年人的肌肉质量也很重要。许多老年人的饮食摄入量和/或血液中几种矿物质(包括钙、镁、硒、铬和锌)水平不足50,51。
一项针对1339名60岁以上韩国成年人的研究报告称,与钙摄入量较低的成年人相比,每日钙摄入量较高与脂肪量显著减少、肌肉量增加和少肌症风险降低有关52。一项针对740名50岁以上塔斯马尼亚成年人的研究报告称,铁、镁、磷、钾和锌的摄入量越高,其手臂和腿部的瘦肌肉量就越大53。动物研究报告称,锌缺乏会降低食欲,较高水平的膳食和补充锌会增加食欲54。
许多恶病质或少肌症患者也会出现骨量减少(骨质疏松症或骨质减少)。一些研究人员指出,少肌症和绝经后骨质疏松症共存,具有非常相似的风险因素,在疾病发展方面表现出相似性,并相互作用55。骨质疏松症大大增加了骨折的风险,髋部和背部骨折通常很少或没有创伤。对63项研究中29项的分析 897名50岁以上的成年人报告称,每天补充800-1500mg钙和400-800IU维生素D可显著降低12%的骨质疏松症相关骨折56。
9.益生菌与慢性腹泻:
艾滋病HIV阳性个体或接受癌症放疗或化疗的人经常经历慢性腹泻,这会显著减少对许多营养物质的吸收。几项研究报告称,使用嗜酸乳杆菌和长双歧杆菌等益生菌可以显著降低艾滋病毒/艾滋病或癌症辐射相关腹泻的发病率57,58。一项针对患有HIV/AIDS相关中度腹泻的女性的研究报告称,在所有12名女性中,每天食用100ml(约3.5盎司)补充有鼠李糖乳杆菌GR1和罗伊氏乳杆菌RC-14的酸奶15天,可以缓解腹泻。每天接受100ml普通酸奶的12名女性中,只有2名(17%)腹泻症状得到缓解。给予两组女性的酸奶最初是用低水平的2种细菌制备的,包括保加利亚德氏乳杆菌和嗜热链球菌57。
对490名接受过结直肠癌或宫颈癌症放射治疗的患者进行了一项大型双盲研究。这些患者接受了含有4500亿活细菌的益生菌补充剂(含有8株益生菌的混合物:ACTIAL益生菌专有品牌VSL#3)或安慰剂在放射治疗期间每天3次。243名接受益生菌治疗的患者中有77名(31.6%)发生了辐射诱导的腹泻,这明显低于239名接受安慰剂治疗的患者(51.8%)中的124名59。
益生菌的混合物在预防腹泻方面可能比单独的益生菌更有用。在对16项已发表的关于益生菌对几种医疗条件(包括肠道健康、预防呼吸道感染、特应性皮炎和腹泻)影响的研究进行综述时,12项研究发现,益生菌混合物比使用单一益生菌菌株更有效60。
10.消化酶:
肌肉萎缩的人也可能受益于口服消化酶补充剂。许多研究报告称,与年轻人相比,老年人的胰腺酶(即消化蛋白质、脂肪和碳水化合物的酶)水平更低61。报告了3名成年人(年龄78至80岁,无胰腺病史)的一系列病例,他们经历了慢性腹泻或呕吐以及严重的体重减轻。服用消化酶后,腹泻和呕吐症状缓解,患者在1至10个月内体重增加了5.9kg至13.6kg62。
另一项研究报告称,在22名服用抗病毒药物并患有慢性腹泻的HIV阳性患者中,有8人的胰腺消化酶水平较低。一名患者在研究期间死于艾滋病毒/艾滋病相关疾病。另外7名患者在接受10, 000至60, 000单位的胰腺酶治疗后,腹泻显著减少63。在另一项针对24名患有严重脂肪吸收不良(即粪便中的脂肪或脂肪泻)的HIV/AIDS患者的研究中,受试者每摄入1g脂肪,就要接受1000单位脂肪酶、800单位淀粉酶和60单位蛋白酶的治疗。经过2周的酶治疗,8名患者(33%)的脂肪吸收不良得到缓解,另外11名患者(46%)的脂肪吸收不良得到显著改善64。
更多内容可点击其个性化的综合干预方案:
- 肌萎缩管理(防止肌肉减少)
- 肌萎缩管理(改善肌肉质量)
- 肌萎缩管理(运动增肌)
- 肌萎缩管理(促进肌肉合成)
- 女性肌萎缩防控(55-65岁)
- 女性肌萎缩防控(66-75岁)
- 女性肌萎缩防控(76岁以上)
- 男性肌萎缩防控(60-70岁)
- 男性肌萎缩防控(71-80岁)
- 男性肌萎缩防控(81岁以上)
以及参阅本网如下专文的有关内容:
医疗干预
在医生监督下,治疗措施包括如下:
- 补充睾酮:包括注射和口服形式。睾酮在肌肉构建中起着关键作用,许多肌肉萎缩的患者(男性和女性)缺乏睾丸激素。
- 补充DHEA:这是性激素的前体物质,有助于提高睾酮水平,增加肌肉合成。
- 补充生长激素:多用于因慢性病(如慢阻肺、艾滋病等)所致的肌肉消耗。
预防
下列方法有助于防止肌肉减少:- 富含饮食蛋白、均衡营养等。
- 保持运动锻炼,包括负重训练、健身运动等。
- 户外活动,快步行走等。
参考文献:
1. Prado CMM et al. Nutrition interventions to treat low muscle mass in cancer. J Cachexia Sarcopenia Muscle. 2020;11(2): 366-380.
2. Antoun S et al. Muscle protein anabolism in advanced cancer patients: response to protein and amino acids support, and to physical activity. Ann Oncol. 2018;29(suppl_2): ii10-ii17.
3. de Campos-Ferraz PL et al. An overview of amines as nutritional supplements to counteract cancer cachexia. J Cachexia Sarcopenia Muscle. 2014;5(2): 105-110.
4. Soares JDP et al. Dietary Amino Acids and Immunonutrition Supplementation in Cancer-Induced Skeletal Muscle Mass Depletion: A Mini-Review. Curr Pharm Des. 2020;26(9): 970-978.
5. Teixeira FJ et al. Whey protein in cancer therapy: A narrative review. Pharmacol Res. 2019;144: 245-256.
6. Engelen MAM et al. High anabolic potential of essential amino acid mixtures in advanced nonsmall cell lung cancer. Ann Oncol. 2015;26(9): 1960-1966.
7. Rondanelli ME et al. Caccialanza and S. Perna. Improving rehabilitation in sarcopenia: a randomized-controlled trial utilizing a muscle-targeted food for special medical purposes. J Cachexia Sarcopenia Muscle. 2020;11(6): 1535-1547.
8. Ahmadi AMH et al. Fortified whey beverage for improving muscle mass in chronic obstructive pulmonary disease: a single-blind, randomized clinical trial. Respir Res.2020;21(1): 216.
9. Pineda-Juárez JA et al. Changes in body composition in heart failure patients after a resistance exercise program and branched chain amino acid supplementation. Clin Nutr. 2016;35(1): 41-47.
10. Orsatti FL et al. Adding Soy Protein to Milk Enhances the Effect of Resistance Training on Muscle Strength in Postmenopausal Women. J Diet Suppl. 2018;15(2): 140-152.
11. Liao YH et al. Soymilk ingestion immediately after therapeutic exercise enhances rehabilitation outcomes in chronic stroke patients: A randomized controlled trial. NeuroRehabilitation. 2019;44(2): 217-229.
12. Devries MC et al. Supplemental protein in support of muscle mass and health: advantage whey. J Food Sci. 2015;80 Suppl 1: A8-a15.
13. van Vliet S et al. The Skeletal Muscle Anabolic Response to Plant- versus Animal-Based Protein Consumption. J Nutr. 2015;145(9): 1981-1991.
14. Devries MC et al. Protein leucine content is a determinant of shorter- and longer-term muscle protein synthetic responses at rest and following resistance exercise in healthy older women: a randomized, controlled trial. Am J Clin Nutr. 2018;107(2): 217-226.
15. Messina M et al. No Difference Between the Effects of Supplementing With Soy Protein Versus Animal Protein on Gains in Muscle Mass and Strength in Response to Resistance Exercise. Int J Sport Nutr Exerc Metab. 2018;28(6): 674-685.
16. Lynch HM et al. No Significant Differences in Muscle Growth and Strength Development When Consuming Soy and Whey Protein Supplements Matched for Leucine Following a 12 Week Resistance Training Program in Men and Women: A Randomized Trial. Int J Environ Res Public Health. 2020;17(11).
17. Rittig N et al. Anabolic effects of leucine-rich whey protein, carbohydrate, and soy protein with and without β-hydroxy-β-methylbutyrate (HMB) during fasting-induced catabolism: A human randomized crossover trial. Clin Nutr. 2017;36(3): 697-705.
18. Babajafari S et al. Comparing isolated soy protein with flaxseed oil vs isolated soy protein with corn oil and wheat flour with corn oil consumption on muscle catabolism, liver function, blood lipid, and sugar in burn patients: a randomized clinical trial. Trials. 2018;19(1): 308.
19. Nikawa T et al. Effects of a soy protein diet on exercise-induced muscle protein catabolism in rats. Nutrition. 2002;18(6): 490-495.
20. Morris CA et al. Attenuation of skeletal muscle atrophy via protease inhibition. J Appl Physiol. 2005;(1985) 99(5): 1719-1727.
21. Paul et al. Evidence Supports the Use of Soy Protein to Promote Cardiometabolic Health and Muscle Development. J Am Coll Nutr. 2015;34 Suppl 1: 56-59.
22. Alexandrov NV et al. Dietary Protein Sources and Muscle Mass over the Life Course: The Lifelines Cohort Study. Nutrients. 2018;10(10).
23. Bhasin S et al. Effect of Protein Intake on Lean Body Mass in Functionally Limited Older Men: A Randomized Clinical Trial. JAMA Intern Med. 2018;178(4): 530-541
24. Miranda JM et al. Egg and egg-derived foods: effects on human health and use as functional foods. Nutrients. 2015;7(1): 706-729.
25. Smith A et al. Considering the benefits of egg consumption for older people at risk of sarcopenia. Br J Community Nurs. 2016;21(6): 305-309.
26. Mobley EB et al. Effects of protein type and composition on postprandial markers of skeletal muscle anabolism, adipose tissue lipolysis, and hypothalamic gene expression. J Int Soc Sports Nutr. 2015;12: 14.
27. Molfino A et al. Beta-hydroxy-beta-methylbutyrate supplementation in health and disease: a systematic review of randomized trials. Amino Acids. 2013;45(6): 1273-1292.
28. Holeček M. Beta-hydroxy-beta-methylbutyrate supplementation and skeletal muscle in healthy and muscle-wasting conditions. J Cachexia Sarcopenia Muscle. 2017;8(4): 529-541.
29. Flakoll P et al. Effect of beta-hydroxy-beta-methylbutyrate, arginine, and lysine supplementation on strength, functionality, body composition, and protein metabolism in elderly women. Nutrition. 2004;20(5): 445-451.
30. Baier S et al. Year-long changes in protein metabolism in elderly men and women supplemented with a nutrition cocktail of beta-hydroxy-beta-methylbutyrate (HMB), L-arginine, and L-lysine. JPEN J Parenter Enteral Nutr. 2009 Jan-Feb;33(1):71-82.
31. Fuller JC et al. Vitamin D status affects strength gains in older adults supplemented with a combination of β-hydroxy-β-methylbutyrate, arginine, and lysine: a cohort study. JPEN J Parenter Enteral Nutr. 2011;35(6): 757-762.
32. Clark R et al. Nutritional treatment for acquired immunodeficiency virus-associated wasting using HMB, glutamine and arginine: A double-blind, placebo controlled study. JPEN - J Parenter Enter Nutr 2000;24(3):133-139.
33. May PE et al. Reversal of cancer-related wasting using oral supplementation with a combination of beta-hydroxy-beta-methylbutyrate, arginine, and glutamine. Am J Surg. 2002 Apr;183(4):471-9.
34. Bear DE et al. β-Hydroxy-β-methylbutyrate and its impact on skeletal muscle mass and physical function in clinical practice: a systematic review and meta-analysis. Am J Clin Nutr. 2019;109(4): 1119-1132.
35. Kinugasa Y et al. Association of carnitine insufficiency with sarcopenia and dynapenia in patients with heart failure. Geriatr Gerontol Int. 2023 Jul;23(7):524-530.
36. Hiramatsu A et al. Levocarnitine Use Is Associated With Improvement in Sarcopenia in Patients With Liver Cirrhosis. Hepatol Commun. 2019 Jan 22;3(3):348-355.
37. Rawson ES et al. Use of creatine and evidence for effects of cognitive function in the young and old. Amino Acids 2011;40(5):1349-1362.
38. Candow DG et al. Low-dose creatine combined with protein during resistance training in older men. Med Sci Sports Exerc 2008;40(9):1645-1652.
39. McGlory C et al. Omega-3 fatty acid supplementation attenuates skeletal muscle disuse atrophy during two weeks of unilateral leg immobilization in healthy young women. The FASEB Journal. 2019;33(3):4586-4597.
40. Smith GI et al. Dietary omega-3 fatty acid supplementation increases the rate of muscle protein synthesis in older adults: a randomized controlled trial. Am J Clin Nutr 2011;93(2):402-412.
41. Robinson SM et al. Diet and its relationship with grip strength in community-dwelling older men and women: the Hertfordshire Cohort Study. J Am Geriatr Soc 2008;56(1):84-90.
42. Wigmore SJ et al. The effect of polyunsaturated fatty acids with the progress of cachexia in patients with pancreatic cancer. Nutrition 1996;12 (supplement 1):S27-S30.
43. Ginde AA et al. Demographic differences and trends of vitamin D insufficiency in the US population. Arch Int Med 2009;169:629-632.
44. Bischoff-Ferrari A et al. Fall prevention with supplemental and active forms of vitamin D: a meta-analysis of randomized controlled trials. BMJ 2009;339:b3692.
45. Dawson-Hughes B. Serum 25-hydroxyvitamin D and functional outcomes in the elderly. Am J Clin Nutr 2008;88(supplement):537S-540S.
46. Tieland M et al. Low vitamin D status is associated with reduced muscle mass and impaired physical performance in frail elderly people. European journal of clinical nutrition. Oct 2013;67(10):1050-1055.
47. Wong YY et al. Low vitamin D status is an independent predictor of increased frailty and all-cause mortality in older men: the Health in Men Study. The Journal of clinical endocrinology and metabolism. Sep 2013;98(9):3821-3828.
48. Rahman MM et al. Conjugated linoleic acid (CLA) prevents age associated skeletal muscle loss. Biochem Biophys Res Commun 2009;383(4):513-518.
49. Tarnopolsky M et al. Creatine monohydrate and conjugated linoleic acid improve strength and body composition following resistance exercise in older adults. PLoS One 2007;2(10):e991.
50. Park S et al. Vitamin and mineral supplements: Barrier and challenges for older adults. J Nutr Elderly 2008;27(3-4):297-317.
51. Vaquero MP. Magnesium and trace elements in the elderly: Intake, status, and recommendations. J Nutr Health Aging 2002;6(2):147-153.
52. Seo MH et al. The association between daily calcium intake and sarcopenia in older, non-obese Korean adults: the Fourth Korea National Health and Nutrition Examination Survey (KNHANES IV) 2009. Endocr J 2013;60(5):679-686.
53. Scott D et al. Associations between dietary nutrient intake and muscle mass and strength in community-dwelling older adults: The Tasmanian older adult cohort study. J Am Geriatr Soc 2010;58:2129-2134.
54. Suzuki H et al. Zinc as an appetite stimulator- the possible role of zinc in the progression of diseases such as cachexia and sarcopenia. Recent Pat Food Nutr Agric 2011;3(3):226-231.
55. Sirola J et al. Similarities in acquired factors related to postmenopausal osteoporosis and sarcopenia. J Osteroporos 2011. Doi: 4061/2011/536735
56. Tang B et al. Use of calcium in combination with vitamin D supplementation to prevent fractures and bone loss in people aged 50 years or older: a meta-analysis. Lancet 2007;370(9844):657-666.
57. Anukam KC et al. Yogurt containing probiotic Lactobacillus rhamnosus GR-1 and L. reuteri RC-14 helps resolve moderate diarrhea and increases CD4 count in HIV/ AIDS patients. J Clin Gastroenterol 2008; 42(3):239-243.
58. Fuccio L et al. Effects of probiotics for the prevention and treatment of radiation-induced diarrhea. J Clin Gastroenterol 2009;43(5):506-513.
59. Delia P et al. Use of probiotics for prevention of radiation-induced diarrhea. World J Gastroenterol 2007;13:912-915.
60. Chapman CMC et al. Health benefits of probiotics: are mixtures more effective than single strains? Eur J Nutr 2011;50:1-17.
61. Holt PR. Intestinal malabsorption in the elderly. Dig Dis 2007;144-150.
62. Coulson JM et al. Pancreatic insufficiency and weight loss in older patients. QJM (Quartely Journal of Medicine) 2004;97:377-380.
63. Price DA et al. Pancreatic exocrine unsufficiency in HIV-positive patients. HIV Medicine 2005;6:33-36.
64. Carrocio A et al. Efficacy of oral pancreatic enzyme therapy for the treatment of fat malabsorption in HIV-infected patients. Aliment Pharmacol Ther 2001;15:1619-1625.
参考来源:
美国国立公众健康网
https://medlineplus.gov
美国医疗在线网
www.webmd.com
维基百科-少肌症
https://en.wikipedia.org/wiki/Sarcopenia
美国国际少肌症论坛
https://frailty-sarcopenia.com/
美国国立卫生研究院
www.nih.gov
免责声明和安全信息
- 本信息(包括任何附带资料)不是为了取代医生或有关合格从业人士的建议或忠告。
- 任何人如果想要对本文涉及的药物、饮食、运动或其他生活方式的使用、或改变调整,以预防或治疗某一特定健康状况或疾病,应首先咨询医生或有关合格从业人士,并获得他/她们的许可。妊娠和哺乳妇女在使用本网站任何内容前,尤其应征求医生的意见。
- 除非另有说明,本网站所述内容仅适用于成人。
- 本网站所推荐的任何产品,消费者应该以实际的产品标签内容为准,尤其应关注重要的安全信息以及产品最新信息,包括剂量、使用方法和禁忌症等。
- 由于循证医学研究、文献及有关产品处于不断的变化中,本网站工作人员将尽力更新。
- 本网站不能保证所载文章内容、综合干预方案以及相关成分或产品述及的健康益处,也不承担任何责任。

